Erfahren Sie in dieser Schulung zum Risikomanagement nach ISO 14971 alles rund um das Risikomanagement sowie die Qualitätssicherung bei der Produktion von medizinischen Geräten. Im Allgemeinen regelt die Norm ISO 14971 zudem Aspekte der Nutzung von elektrischen Gerätschaften in medizinischer Praxis. Die Norm ist also für Risikomanagement in Produktionsunternehmen ausgelegt, deren Endprodukte (elektrische Geräte und Zubehör) in der Medizin eingesetzt werden, wodurch erhöhte Risiken resultiert. Durch die Ausrichtung Ihres Betriebes nach der Norm ISO 14971 werden Sie Kundenanforderungen gerecht und sorgen für Rechtssicherheit durch die Erfüllung der Anforderungen der Norm ISO 14971 in Ihrem Unternehmen.
Die Schulung hilft Ihnen die Norm ISO 14971 kennen zu lernen und vor allem richtig zu interpretieren! Die Norm formuliert Anforderungen für die Bewertung der Risiken, für die Risikosteuerung und die Auswertung der Informationen der Kunden oder Dritter über die Nutzung der medizinischen Geräten. Damit ist bspw. das Beschwerdemanagement gemeint, welches die Berücksichtigung der Fehler und die zukünftige Vermeidung dieser sicherstellen soll. Die Norm ISO 14971 erlaubt es den Produzenten von medizinischen Geräten, die Risiken, die mit der Nutzung von diesen in der medizinischen Praxis einhergehen, einzuschätzen sowie anschließend abzuwägen. Das alles lernen Sie in dem Risikomanagement Seminar Medizinprodukte!

Welche Inhalte vermitteln wir Ihnen in der Risikomanagement ISO 14971 Schulung?
Durch die EN ISO 13485 sowie die Medizinprodukteverordnung MDR wird ein funktionierendes Risikomanagement immer wichtiger. Nachfolgend erhalten Sie die Übersicht zu den Inhalten dieser Risikomanagement ISO 14971 Schulung.
Grundlagen des Risikomanagement nach ISO 14971
Zu Beginn lernen Sie in dieser Schulung alle Grundlagen zum Risikomanagement für Medizinproduktehersteller kennen. Hierbei lernen Sie zunächst einmal die grundlegenden sowie die neuen Anforderungen an ein Risikomanagement kennen.
- Grundlegende Anforderungen des Risikomanagements nach ISO 14971
- Neue Anforderungen an das Risikomanagement
- Risikoanalyse auf Basis der neuen Anforderungen
- Verschiedene Verfahren der Risikoanalyse
- Potenzielle und akute Gefährdungen erkennen
Welche regulatorischen Anforderungen gibt es an das Risikomanagement?
Schließlich lernen Sie in dieser Schulung, wie Sie Risiken richtig einschätzen und bewerten. Zudem lernen Sie die Risikobewertung sowie die Risikokontrolle kennen.
- Risiken richtig einschätzen und verhindern
- Risikobewertung und Risikokontrolle
- Bewertung des Restrisikos
- Der Risikomanagementbericht
- Die Marktbeobachtung
Welche Ziele und Zielgruppe hat diese Risikomanagement ISO 14971 Schulung?
Sie lernen in dieser Schulung ein Risikomanagement ISO 14971 für Medizinprodukte entsprechend den relevanten gesetzlichen Anforderungen der MDR unter Anwendung der DIN EN ISO 14971 zu betreuen. Sie lernen, eine Risikoanalyse durchzuführen und können danach potenzielle und akute Gefährdungen feststellen, Risiken richtig einschätzen und verhindern. Dieses Seminar ist für diejenigen gedacht, die für das Risikomanagement eines Medizinprodukte Herstellers verantwortlich sind und dabei eine Risikoanalyse nach ISO 14971 durchführen müssen. Das sind zum Beispiel Führungskräfte, Fachpersonal, Qualitätsmanagementbeauftragte sowie Qualitätsleiter, die die Verantwortung für den Aufbau von Qualitätsmanagementsystemen tragen.
Für Ihre Teilnahme an diesem Seminar sind keine speziellen Vorkenntnisse vorausgesetzt.
Was für einen Zertifikat gibt es im Anschluss an Ihre Teilnahme?
Nach der Teilnahme an dieser Schulung Risikomanagement Medizinprodukte Schulung ISO 14971 erhalten Sie eine Qualifikationsbescheinigung in Deutsch sowie in Englisch.
Alle Informationen zu dieser Risikomanagement ISO 14971 Schulung
 Weitere Infos, Termine & Anmeldung
Weitere Infos, Termine & Anmeldung
Hier erhalten Sie Infos zu den Preisen, den nächsten Terminen und den Veranstaltungsorten in Ihrer Nähe! Sie möchten diese Schulung besuchen? Dann melden Sie sich gleich zu Ihrem Wunschtermin an!
 Download der Schulungsinhalte
Download der Schulungsinhalte
Laden Sie sich die Inhalte des Seminars Risikomanagementbeauftragter ISO 31000 kostenfrei als PDF-Datei herunter. Informieren Sie sich über diese und weitere Schulungen aus unserem Ausbildungsprogramm!
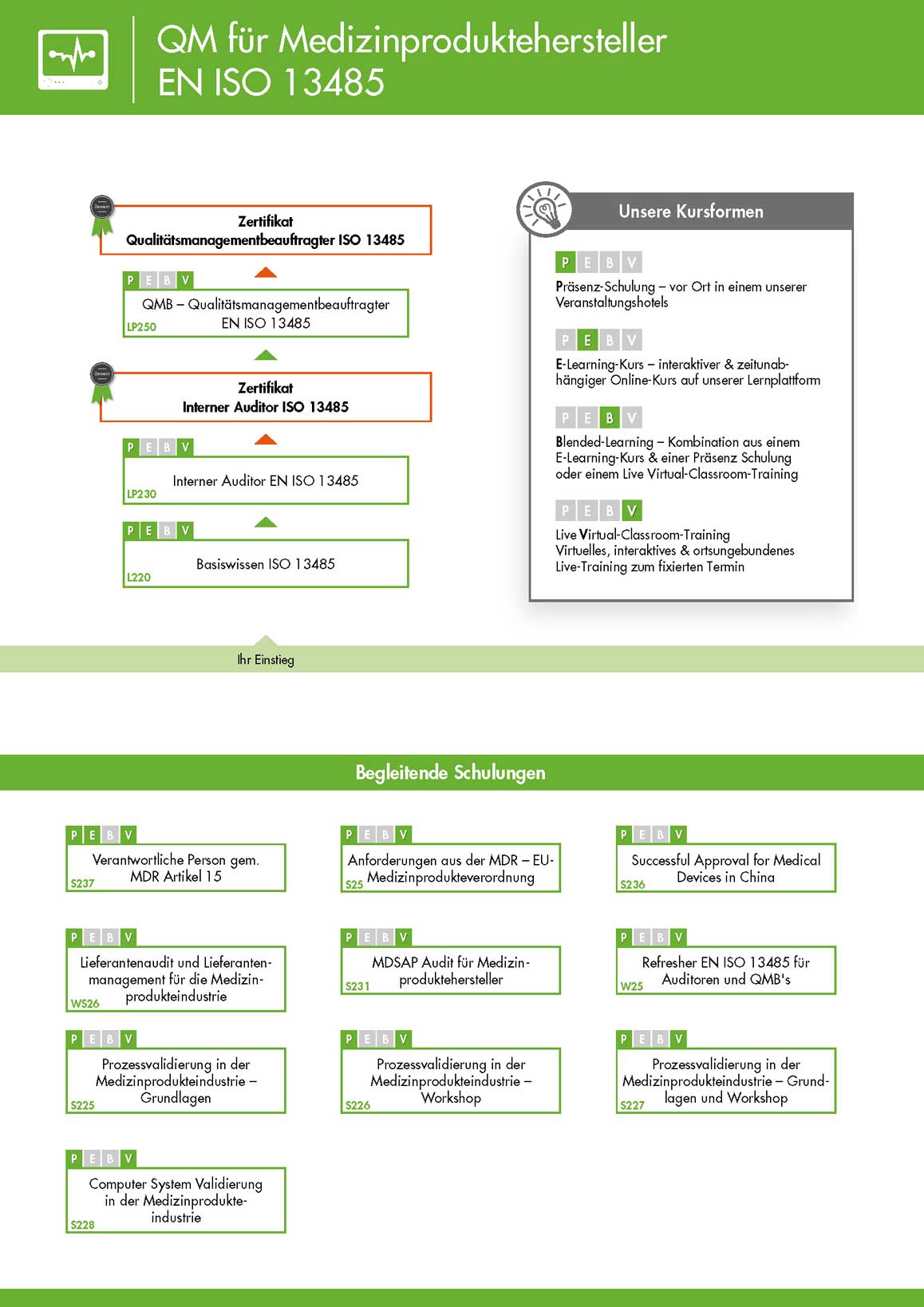
Weiterbildung zum Qualitätsmanagement für Medizinprodukte – Ihre Übersicht
Die Ausbildung im Bereich Medizinprodukte ist z.T modular aufgebaut, z.T. handelt es sich um individuelle Seminare. Somit ist Ihr individueller Einstieg möglich. Abhängig davon, ob Sie bereits über Vorkenntnisse verfügen oder nicht, können Sie Ihre Ausbildung ganz Ihren Bedürfnissen anpassen. DOWNLOAD Ausbildungsprogramm: Klicken Sie auf den Link, um sich unsere umfangreiche Übersicht als PDF herunterzuladen.
Sie sehen in unserer Schulungsübersicht außerdem, in welcher Kursform das jeweilige Modul zur Verfügung steht. Dabei gibt es Präsenztraining, Blended Learning und Online Schulung in Form von E-Learning als Möglichkeiten.
Klicken Sie auf die Grafik, um diese vergrößert anzuzeigen.